
A Agência Nacional de Vigilância Sanitária (Anvisa) informou hoje (6/06) que aguarda documentos do Instituto Butantan para avaliar o pedido de início de estudos com seres humanos para o desenvolvimento da vacina brasileira Butanvac.

De acordo com a Anvisa, este momento em que são necessárias informações complementares constituem a fase do processo se que o órgão chama de "exigência". Ainda segundo a Agência, o Instituto Butantan se comprometeu a fornecer os dados faltantes até amanhã (7/06).
O pedido foi apresentado no dia 26 de março. Conforme a Anvisa, desde esta data durante 48 dias os técnicos aguardaram informações complementares. Os últimos dados recebidos foram sobre o protocolo clínico, que estão sendo analisados pela equipe técnica da Agência.
O esclarecimento foi divulgado após notícias publicadas em meios de comunicação sobre uma suposta iminência da autorização dos estudos pela Anvisa.
Saiba Mais
-
![]() Brasil
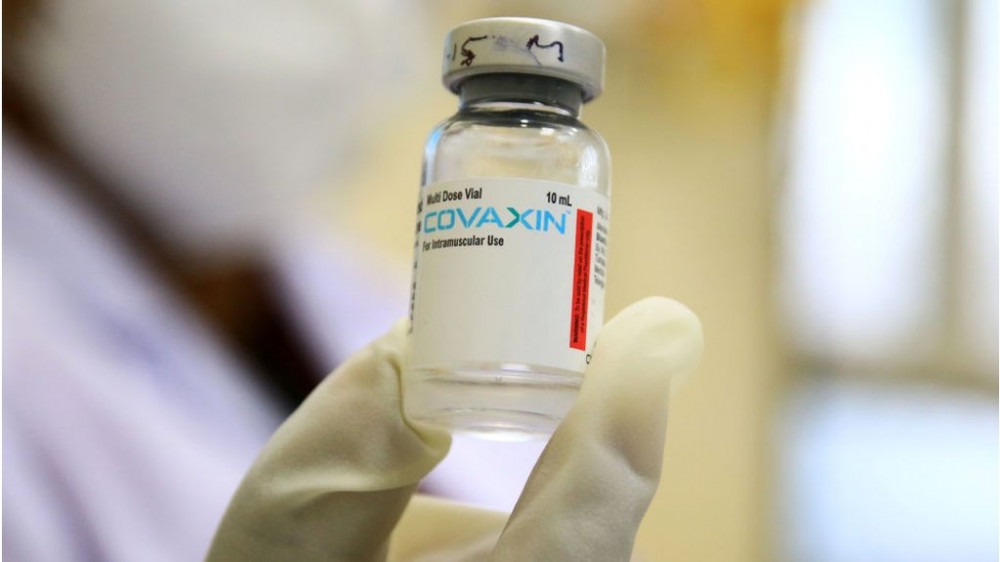
Covaxin e Sputnik V: O que muda na vacinação do Brasil com decisão da Anvisa
Brasil
Covaxin e Sputnik V: O que muda na vacinação do Brasil com decisão da Anvisa
-
![]() Brasil
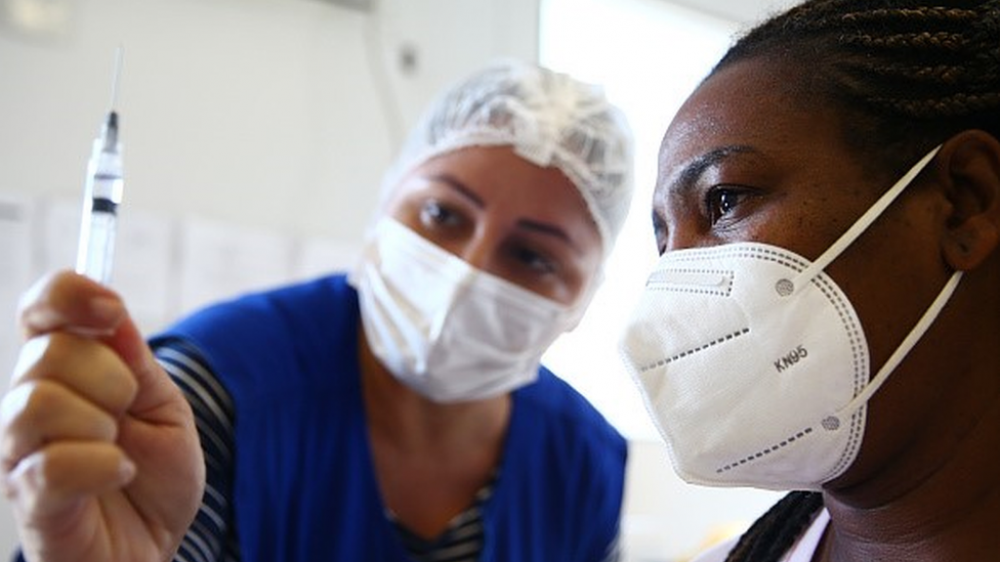
CoronaVac, AZD1222, Cominarty, Ad26.COV2-S, Sputnik e Covaxin: compare as seis vacinas com aval da Anvisa
Brasil
CoronaVac, AZD1222, Cominarty, Ad26.COV2-S, Sputnik e Covaxin: compare as seis vacinas com aval da Anvisa
-
![]() Política
Governadores do Norte, Nordeste e Centro-Oeste se reúnem para tratar da Sputnik V
Política
Governadores do Norte, Nordeste e Centro-Oeste se reúnem para tratar da Sputnik V
-
![]() Brasil
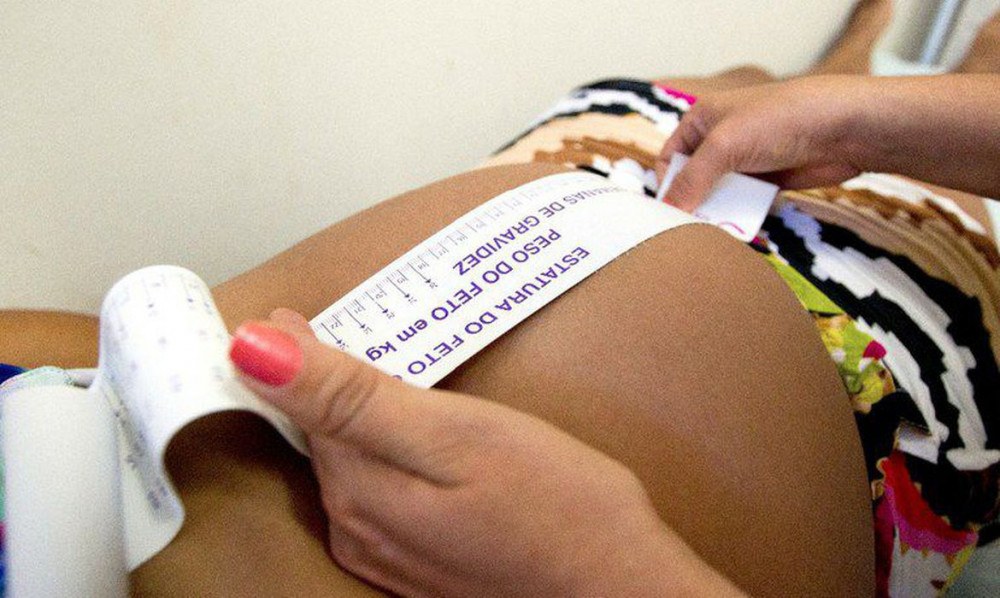
Morte de grávidas por covid em 5 meses já supera 2020; letalidade está em alta
Brasil
Morte de grávidas por covid em 5 meses já supera 2020; letalidade está em alta
-
![]() Mundo
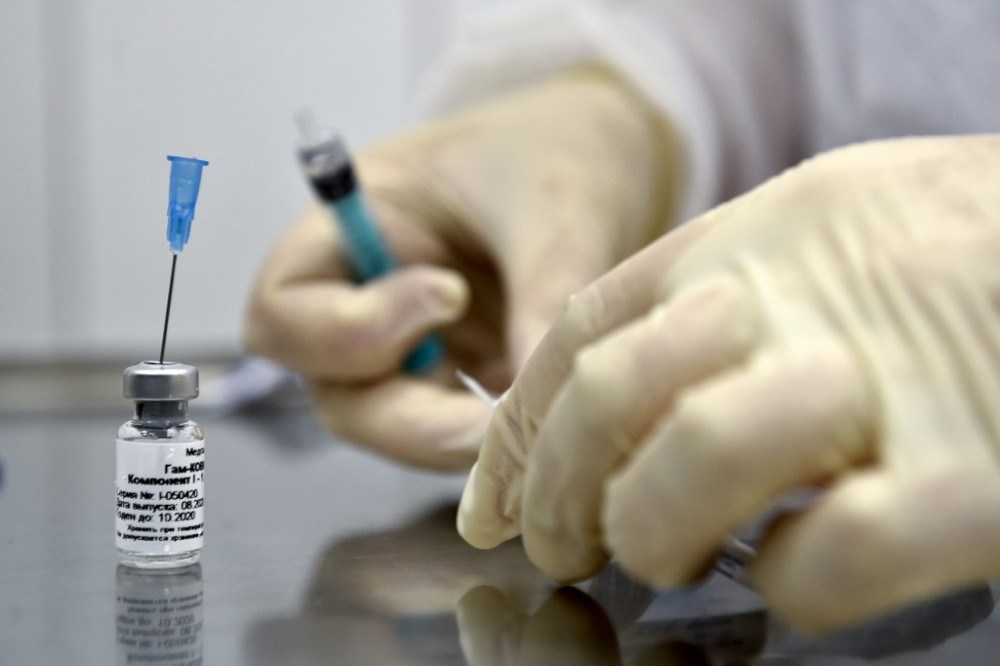
Variante de covid-19 identificada na Índia é 40% mais contagiosa, diz ministro da Saúde britânico
Mundo
Variante de covid-19 identificada na Índia é 40% mais contagiosa, diz ministro da Saúde britânico
-
![]() Brasil
Aval restrito dado pela Anvisa para Sputnik V desagrada a Estados
Brasil
Aval restrito dado pela Anvisa para Sputnik V desagrada a Estados
Notícias pelo celular
Receba direto no celular as notícias mais recentes publicadas pelo Correio Braziliense. É de graça. Clique aqui e participe da comunidade do Correio, uma das inovações lançadas pelo WhatsApp.
Dê a sua opinião
O Correio tem um espaço na edição impressa para publicar a opinião dos leitores. As mensagens devem ter, no máximo, 10 linhas e incluir nome, endereço e telefone para o e-mail sredat.df@dabr.com.br.
 Brasil
Brasil
 Brasil
Brasil
 Política
Política
 Brasil
Brasil
 Mundo
Mundo
 Brasil
Brasil