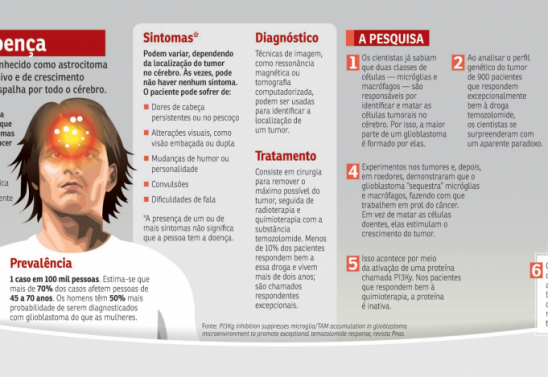
O diagnóstico de glioblastoma multiforme, ou de grau IV, oferece, hoje, poucas expectativas de tratamento eficaz. Diferentemente do tipo de câncer cerebral, que começa menos agressivo e evolui aos poucos, esse é resistente aos quimioterápicos, reduzindo as chances de uma sobrevida mais longa. Porém, um pequeno grupo de pacientes — menos de 10% — reage bem aos medicamentos e vive, no mínimo, três vezes mais que a média das pessoas com a doença. Neles pode estar a esperança de uma nova abordagem terapêutica, segundo um estudo publicado na revista Proceedings of the National Academy of Sciences (Pnas).
Os chamados respondentes excepcionais são considerados o calcanhar de Aquiles de diversos tipos de câncer cujo prognóstico não é favorável. Esses pacientes estão oferecendo pistas para as bases de um tratamento personalizado, voltado para a correção de mutações genéticas. No caso do glioblastoma, essas peças que faltam no quebra-cabeça são fundamentais porque a expectativa de vida após o diagnóstico é de apenas 15 meses, em média. Na literatura médica, há relatos, porém, de pessoas que viveram mais de 10 anos com a doença.
Para desvendar o alvo de um futuro tratamento eficaz para o glioblastoma, pesquisadores da Faculdade de Medicina da Universidade de Minnesota, nos EUA, estudaram o perfil genético do tumor de 900 respondentes excepcionais. As informações estavam em bancos de dados mundiais e foram reunidas pela equipe liderada por Clark Chen, chefe do Departamento de Neurologia e principal autor do estudo. “A base molecular dessas respostas excepcionais pode ser a chave para transformar a esperança de ‘milagres’ em uma verdadeira cura para pacientes com glioblastoma”, diz.
O tratamento desse câncer exige uma cirurgia para retirada da maior parte possível do tumor. Essas amostras são perfiladas geneticamente e suas informações, compartilhadas em bancos de dados. Aaron Sarver, do Instituto de Informática em Saúde da Universidade de Minnesota, utilizou técnicas avançadas de análise das informações para descobrir o que havia de diferente nos tecidos cancerosos dos pacientes excepcionais. As pistas estavam em células que têm como missão reconhecer e matar aquelas que não deveriam estar presentes no cérebro saudável, as micróglias e os macrófagos.
Esses grupos celulares fazem parte do sistema imunológico e são especializados na caça ao câncer. Normalmente, elas migram para locais em que há células cancerosas e as cercam, o que explica por que mais da metade de uma amostra de glioblastoma seja composta por micróglias e macrófagos. A expectativa dos cientistas era de que, nos pacientes excepcionais, houvesse uma quantidade ainda maior. “Se a microglia e os macrófagos normalmente protegem contra as células cancerosas, ter um número maior delas deveria fazer com que o organismo protegesse melhor o tumor. Portanto, esperávamos ver mais delas em respondedores excepcionais. No entanto, descobrimos o contrário”, diz Jun Ma, pesquisador do Departamento de Neurocirurgia e coautor do estudo.
O que os cientistas viram foi uma estratégia inteligente das células cancerosas. Em vez de serem perseguidas e mortas pelas do sistema imunológico, elas conseguem reprogramar micróglias e macrófagos para que eles se tornem aliados. Assim, as células do sistema imunológico ajudam a promover o crescimento do tumor.
“É assustador considerar a possibilidade de que as células cancerosas possam fazer uma ‘lavagem cerebral’ em nossas próprias células imunológicas e convertê-las de células que lutam contra o câncer nas que promovem o câncer”, afirma, em nota, Judith Varner, coautora sênior do estudo e professora de patologia na Universidade da Califórnia, em San Diego. “Felizmente, descobrimos como as células de glioblastoma subvertem nosso sistema imunológico e, agora, podemos reverter essa versão celular da ‘síndrome de Estocolmo’”, compara. A síndrome de Estocolmo é uma reação psicológica que ocorre quando reféns ou vítimas de abusos se aliam aos sequestradores/abusadores para protegê-los.
O perfil genético dos tumores dos pacientes excepcionais revelou que as células tumorais dessas pessoas têm uma mutação no gene PI3Ky, já associada anteriormente a alguns tipos de câncer. A ativação da proteína é que transforma micróglias e macrófagos em aliados do câncer. Nesses pacientes, a PI3Ky não estava ativada. Drogas capazes de silenciá-la, em tese, poderiam devolver às células do sistema imunológico sua função original.
Para testar a hipótese, os cientistas fizeram estudos com modelos camundongos com glioblastoma. Medicamentos desenvolvidos no laboratório de Judith Varner foram capazes de desativar o gene. Isso fez com que os animais respondessem bem à quimioterapia, indicando que a abordagem poderia transformá-los em respondentes excepcionais. “Em nossos modelos animais de glioblastoma, o tratamento com drogas direcionadas ao PI3Ky resultou consistentemente em respostas impressionantemente duráveis à quimioterapia. Estamos ansiosos para traduzir essas descobertas em um teste em humanos, com a esperança de transformar cada paciente de glioblastoma em um paciente excepcional”, diz Chen.