Uma equipe de inspetores, designados pela Agência Nacional de Vigilância Sanitária (Anvisa), já está na China em missão para vistoriar as empresas Sinovac e Wuxi Biologics, envolvidas nas pesquisas de vacinas contra a covid-19. A viagem será até 11 de dezembro.
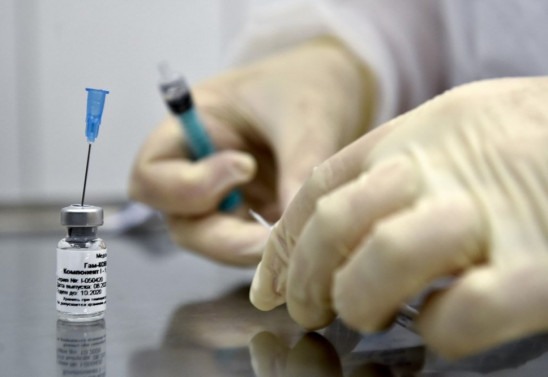
Ontem (30/11), no primeiro dia de inspeção, eles verificaram as práticas de fabricação da vacina CoronaVac, da Sinovac, que está em fase de testes no Brasil, em parceria com o Instituto Butantan. Caso seja eficaz, o órgão passará a fabricar a vacina com os insumos da Sinovac e, posteriormente, com insumos próprios.
Foram analisados os pontos do sistema de gestão da qualidade farmacêutica da empresa, como o gerenciamento de risco, gerenciamento de documentos e plano mestre de validação, além dos requisitos técnicos dos bancos de sementes e celulares (partículas virais e células hospedeiras utilizadas na fabricação da vacina).
Procedimentos de amostragem
De acordo com a Anvisa, outra parte da equipe dedicou-se à verificação das condições aplicáveis aos procedimentos de amostragem de matérias-primas, qualificação de fornecedores, sistema de numeração de lotes e qualificação de transporte.
Em comunicado, a Anvisa esclareceu que a equipe segue uma agenda de trabalho que se estenderá até sexta-feira (4/12) na empresa Sinovac.
"O cronograma inclui em cada dia diferentes requisitos técnicos a serem constatados para avaliar se a fabricação da vacina transcorre de acordo com o regulamento de Boas Práticas da Agência, o qual está a par e passo com os regulamentos utilizados pelas principais agências sanitárias internacionais", informou a agência reguladora.
Do dia 7 ao dia 11, a equipe estará na Wuxi Biologics, que produz os insumos para a vacina da farmacêutica AstraZeneca, que está desenvolvendo o imunizante em parceria com a Universidade de Oxford. Essa vacina também está sendo testada no Brasil e, em caso de sucesso, será fabricada no país pela Fundação Oswaldo Cruz (Fiocruz), do Ministério da Saúde.