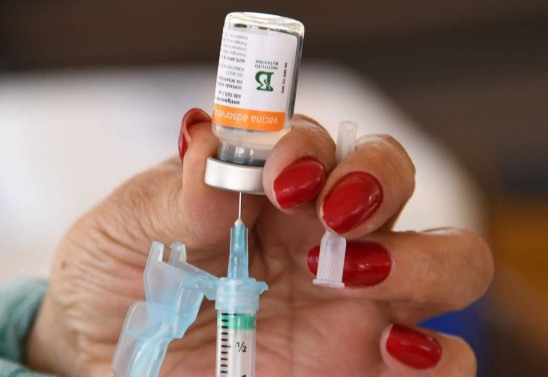
A Anvisa aprovou, ontem, a aplicação da vacina CoronaVac em crianças entre três e cinco anos de idade. A medida foi aprovada pela Diretoria Colegiada, por unanimidade. A conclusão foi de que, apesar dos estudos serem preliminares, os benefícios conhecidos e potenciais do imunizante são muito superiores aos riscos.
Estudos mostram que a CoronaVac criou mais anticorpos contra a covid-19 em crianças — até então era aplicada para menores acima de seis anos — do que em adultos. Diretora da Anvisa e relatora do processo, Meiruze Sousa Freitas argumentou em defesa da aplicação do medicamento em crianças que a capacidade de uma vacina de proteger da mortalidade e contra doenças graves é o principal parâmetro de relevância para a avaliação da eficácia. E lembrou que as internações hospitalares e os cuidados intensivos representam uma pesada carga para o sistema de saúde.
"A covid-19 se apresentou como uma crise universal e, para algumas crianças, o impacto será para toda vida. Apesar de não serem o rosto da pandemia, elas podem estar entre as maiores vítimas. Sabemos que todas, nos diversos países, estão sendo afetadas, mas os efeitos nocivos serão sentidos nos mais vulneráveis, tanto os mais vulneráveis economicamente quanto os com saúde mais debilitada", salientou Meiruse.
Gustavo Mendes, gerente-geral de Produtos Biológicos da Anvisa, votou favoravelmente à aprovação da aplicação em crianças entre três e cinco anos, mas ressaltou a importância da continuidade nos estudos. Ele ainda apresentou a posição das sociedades brasileiras de Pediatria, de Imunizações, de Infectologia, de Pneumologia e de Tisiologia — todas favoráveis à aplicação.
"Os benefícios da vacinação na população de crianças de três a cinco anos, com a vacina CoronaVac/Sinovac-Butantan (particularmente pela expectativa de redução do risco de hospitalizações), superam os eventuais riscos associados à vacinação, no contexto atual da pandemia", salientaram na argumentação junto à Anvisa.
*Estagiária sob a supervisão de Fabio Grecchi