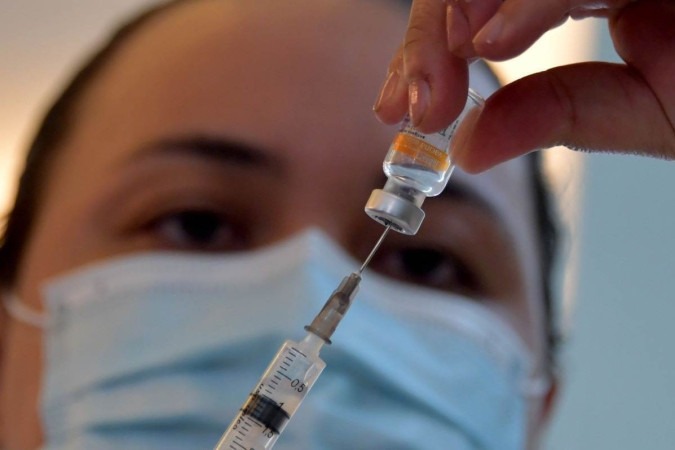
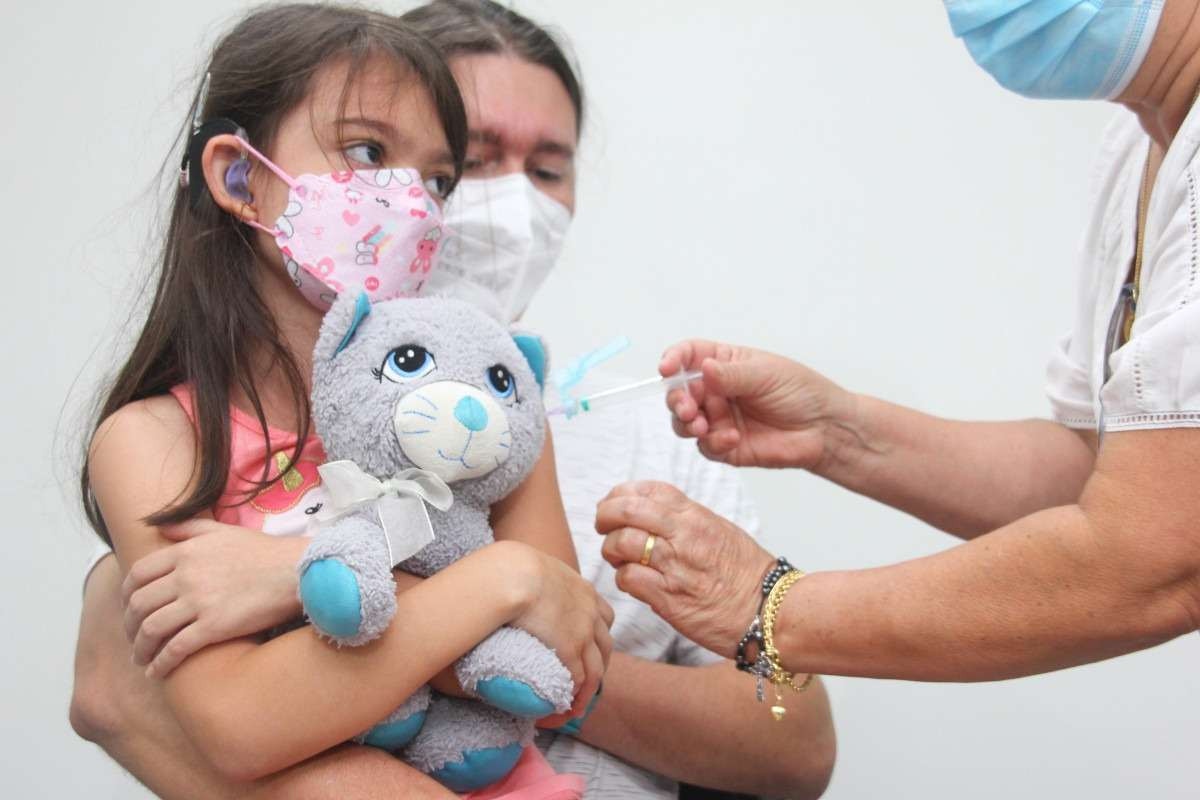
Técnicos da Agência Nacional de Vigilância Sanitária (Anvisa) e do Instituto Butantan se reuniram, na tarde desta segunda-feira (17/1), para debater a respeito da liberação da vacina Coronavac para crianças e adolescentes entre 3 a 17 anos. O encontro não teve caráter decisório, ainda se trata de recolhimento de informações para a tomada de decisão.
Foi apresentada parte da análise, realizada a partir de dados protocolados pelo Butantan. Além disso, os especialistas discutiram sobre as novas fases para a avaliação do processo da Coronavac, que começou desde o dia 15 de dezembro.
Nesta terça-feira (18/01), a Anvisa receberá os relatórios da Sociedade Médica Brasileira, fruto da reunião técnica realizada na semana passada. Sem direito a voto, essa é a contribuição que a instituição ofereceu para o processo.
A partir disso, a área técnica da Anvisa irá redigir um relatório final unindo as informações de todas as participações nas análises. O documento será encaminhado para a diretora relatora, responsável por agendar uma nova reunião com a diretoria colegiada, em caráter extraordinário, para a votação em maioria simples.
Por se tratar de permissão em uso emergencial, a decisão é da diretoria colegiada e embasada em subsídios apresentados pela Gerência-Geral de Medicamentos e Produtos Biológicos (GGMED) e pela Gerência de Farmacovigilância (GFARM). A reunião ainda não tem data prevista.
Saiba Mais
Notícias pelo celular
Receba direto no celular as notícias mais recentes publicadas pelo Correio Braziliense. É de graça. Clique aqui e participe da comunidade do Correio, uma das inovações lançadas pelo WhatsApp.
Dê a sua opinião
O Correio tem um espaço na edição impressa para publicar a opinião dos leitores. As mensagens devem ter, no máximo, 10 linhas e incluir nome, endereço e telefone para o e-mail sredat.df@dabr.com.br.
 Brasil
Brasil
 Brasil
Brasil
 Brasil
Brasil
 Brasil
Brasil