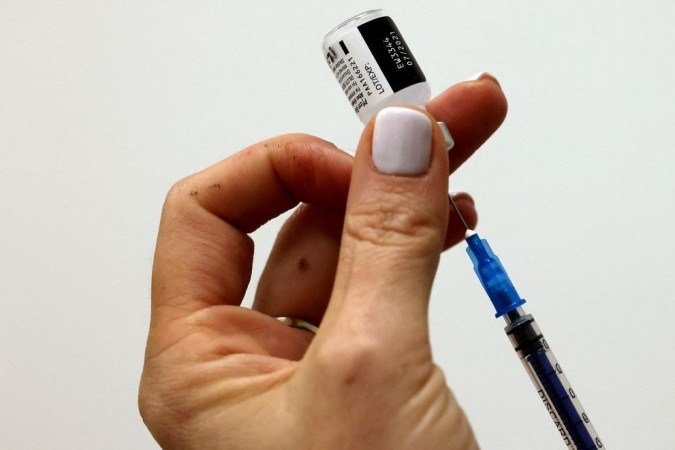
A Agência Nacional de Vigilância Sanitária (Anvisa) realizou, nesta quinta-feira (19/8), uma reunião com o laboratório americano Pfizer para discutir e solicitar os dados científicos disponíveis até o momento sobre a necessidade de uma dose de reforço da vacina da Pfizer, especialmente para pacientes transplantados e imunossuprimidos.
“A reunião foi chamada pela agência, que quer ter acesso aos dados de estudos conduzidos pela empresa na medida em que se tornem disponíveis no mundo. O objetivo é acompanhar todos os dados, tanto aqueles que fazem parte das pesquisas diretas conduzidas pela Pfizer quanto de outras publicações que possam contribuir com a avaliação sobre necessidade de dose de reforço”, afirmou o órgão regulador em nota.
A decisão sobre a recomendação da terceira dose ainda está em análise. Até o momento não há solicitação formal da Pfizer sobre a inclusão de doses de reforço na bula da vacina Comirnaty. De acordo com a diretora da Anvisa, responsável pela área de medicamentos e vacinas, Meiruze Freitas, a agência visa “olhar à frente e antecipar a discussão sobre doses de reforço''. Segundo a diretora, a principal questão é entender se e quando as doses serão necessárias, o que pode ter impacto no esquema de imunização em uso no país.
No encontro, ficou acordado que a Anvisa e a Pfizer terão uma agenda permanente para acompanhar os dados que estão sendo levantados em torno de uma possível dose de reforço.
CoronaVac
Na quarta-feira (18), o órgão recomendou que o Ministério da Saúde avalie aplicar uma dose de reforço (ou seja, uma terceira dose) da vacina CoronaVac para pacientes imunossuprimidos e idosos, especialmente, acima de 80 anos.
De acordo com a Anvisa, o Instituto Butantan, responsável pela produção da vacina em parceria com o laboratório chinês Sinovac, ainda não solicitou a análise. A medida seria uma antecipação do órgão regulador na recomendação, com intenção de frear o avanço da variante Delta no país.
*Estagiária sob a supervisão de Andreia Castro
Saiba Mais
Notícias pelo celular
Receba direto no celular as notícias mais recentes publicadas pelo Correio Braziliense. É de graça. Clique aqui e participe da comunidade do Correio, uma das inovações lançadas pelo WhatsApp.
Dê a sua opinião
O Correio tem um espaço na edição impressa para publicar a opinião dos leitores. As mensagens devem ter, no máximo, 10 linhas e incluir nome, endereço e telefone para o e-mail sredat.df@dabr.com.br.
 Ciência e Saúde
Ciência e Saúde
 Ciência e Saúde
Ciência e Saúde