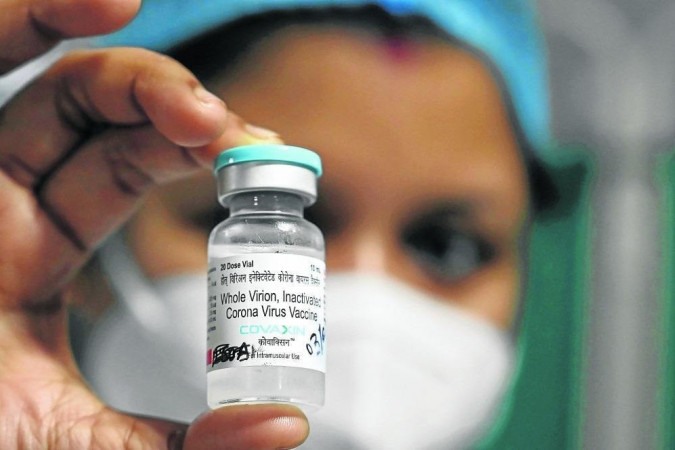
A Agência Nacional de Vigilância Sanitária (Anvisa) negou, nesta quarta-feira (31/3), autorização excepcional e temporária para importação e distribuição da vacina Covaxin, produzida pela Bharat Biotech International. A decisão foi garantida por unanimidade já que os cinco diretores que compõem a Diretoria Colegiada da agência votaram contra a importação do imunizante.
A decisão ocorre um dia após a agência negar a certificação de boas práticas de fabricação à empresa. A negativa do documento, necessário para a obtenção do registro de remédios e imunizantes no Brasil, não impediria a importação excepcional da Coxaxin, mas foi usada para basear os votos dos diretores da agência.
Na justificativa, o relator da 5ª diretoria da Anvisa e relator do processo, Alex Machado Campos, apontou inconsistência na documentação, com lacunas importantes para garantir que a eficácia, segurança e qualidade da vacina, tal como descrita no estudo clínico, possam ser cumpridas. Segundo Campos, "a área técnica identifica riscos e incertezas no uso da vacina Covaxin nas condições atuais", de maneira que não foi possível determinar "a relação benefício risco da com as informações disponíveis até o momento".
Campos sustentou que a concessão, da forma com que o processo se encontra, fere a lei 14.124/21, que estabeleceu as diretrizes de importação e uso emergencial, e, o que significa colocar em risco a segurança da população. "Não entregar a quantidade de antígenos necessário para gerar a resposta imune pode agravar a situação epidêmica, levando a um relaxamento das medidas de contenção e ao aparecimento de novas variantes", destacou o relator, ao votar contrariamente à possibilidade de importação.
Outros diretores, como a diretora da 2ª diretoria da Anvisa, Meiruze Freitas, apontaram que com os elementos até agora apresentados não haveria possibilidade de aprovação. “Sempre no sentido da segurança do uso da nossa população por produto de qualidade com eficácia e segurança”, disse Meiruze.
A diretora ressaltou que a Anvisa está de portas abertas para qualquer outro tipo de pedido da empresa Bharat Biotech. “Não existe porta fechada para nenhuma vacina, mas no momento há necessidade de apresentação de adequação quanto às condições de boas práticas de fabricação que estão diretamente ligadas à segurança e à qualidade da vacina”, completou.
Saiba Mais
Notícias pelo celular
Receba direto no celular as notícias mais recentes publicadas pelo Correio Braziliense. É de graça. Clique aqui e participe da comunidade do Correio, uma das inovações lançadas pelo WhatsApp.
Dê a sua opinião
O Correio tem um espaço na edição impressa para publicar a opinião dos leitores. As mensagens devem ter, no máximo, 10 linhas e incluir nome, endereço e telefone para o e-mail sredat.df@dabr.com.br.
 Brasil
Brasil
 Brasil
Brasil