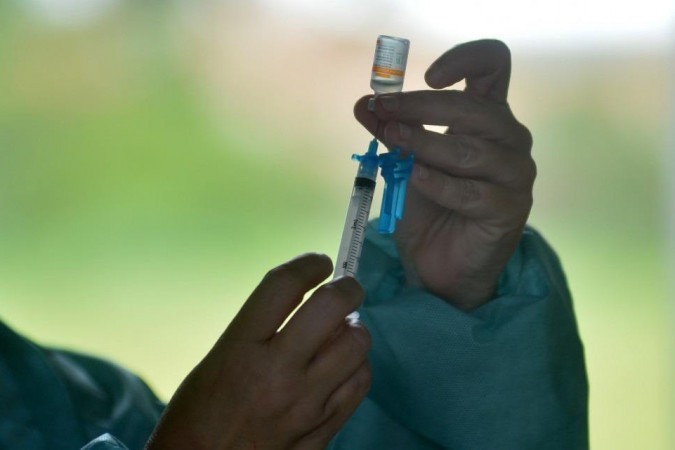
No mesmo dia em que o Instituto Butantan anunciou que protocolará pedido para iniciar estudos clínicos da batizada ButanVac, vacina produzida integralmente no Brasil, o governo federal informou, nesta sexta-feira (26/3), que já solicitou à Agência Nacional de Vigilância Sanitária (Anvisa) a autorização para realizar testes clínicos em humanos da primeira vacina brasileira, financiada pelo governo federal, a Versamune-CoV-2FC.
“O Ministério da Ciência, Tecnologia e Inovações investiu em 15 protocolos, 15 tecnologias diferentes de vacinas aqui no Brasil. Agora, a boa notícia é que três dessas vacinas fizeram os testes com animais e agora estão entrando para fase de testes com pacientes voluntários, ou seja, com testes clínicos”, explicou o ministro da Ciência, Tecnologia e Inovações, Marcos Pontes.
Apesar do pódio, Pontes informou que quem lidera a corrida é a Versamune-CoV-2FC, desenvolvida pela Faculdade de Medicina de Ribeirão Preto (FMRP) junto à empresa brasileira de biotecnologia Farmacore e em parceria com a PDS Biotechnology Corporation. A documentação para para realizar testes clínicos de fase 1 e 2 no Brasil foi protocolada na quinta-feira (25), junto à Anvisa.
“Temos os recursos para financiar esses testes clínicos, que vão ser feitos com 360 pessoas", disse o ministro, completando que, nesta fase, o objetivo é avaliar a segurança da vacina. "Logo depois dele entram os testes clínicos fase 3, que já são realizados com 20 a 30 mil pessoas para testar a eficiência da vacina", completou.
A Farmacore informou que o diálogo junto ao órgão regulador teve início em 6 de novembro de 2020, mas foi só agora que recebeu o sinal verde para dar prosseguimento e encaminhar a documentação. "Estamos entusiasmados em continuar avançando na parceria com a PDS Biotech e em ter o apoio da Anvisa para continuar os estudos que permitam desenvolver um tratamento no Brasil na luta contra esta pandemia", declarou a CEO da Farmacore, Helena Faccioli.
A Anvisa confirmou ter recebido o pedido para testes clínicos de fase 1 e 2 da Versamune-CoV-2FC.
Testes não-clínicos
Ainda no aguardo da aprovação para ser testada em humanos, o imunizante a Versamune-CoV-2FC obteve resultados dos estudos não-clínicos, sobre toxicidade e imunogenicidade, que “demonstram qualidade e competitividade para ser um sucesso nacional e global no controle da covid-19”, segundo o governo federal.
“A vacina demonstrou capacidade de ativar todo o sistema imunológico — imunidade humoral, celular e inata, induzir memória imunológica e proteção de longo prazo”, diz a nota do Ministério da Ciência, Tecnologia e Inovações (MCTI).
Saiba Mais
Notícias pelo celular
Receba direto no celular as notícias mais recentes publicadas pelo Correio Braziliense. É de graça. Clique aqui e participe da comunidade do Correio, uma das inovações lançadas pelo WhatsApp.
Dê a sua opinião
O Correio tem um espaço na edição impressa para publicar a opinião dos leitores. As mensagens devem ter, no máximo, 10 linhas e incluir nome, endereço e telefone para o e-mail sredat.df@dabr.com.br.
 Brasil
Brasil
 Política
Política