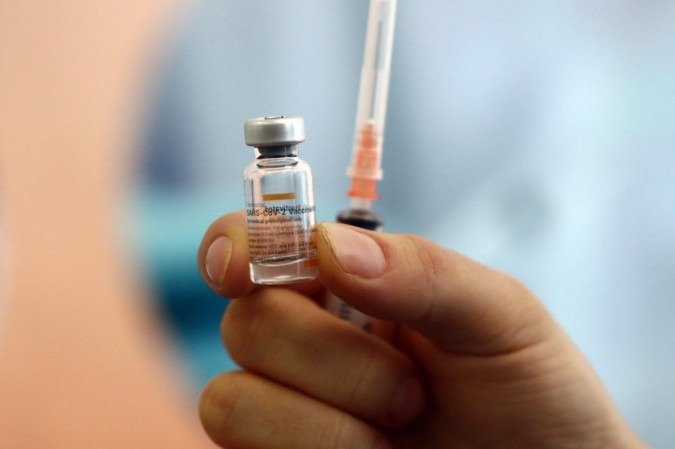
O pedido de registro da CoronaVac, vacina chinesa desenvolvida pela farmacêutica Sinovac e pelo Instituto Butantan, deve ser protocolado nos próximos dias, assim que a documentação apresentada na China e o parecer da agência regulatória do país forem traduzidos para o português. A informação é do diretor do Butantan, Dimas Covas, e foi repassada durante coletiva nesta quarta-feira (10/2), com a atualização das medidas contra a covid-19 do estado de São Paulo.
"Aconteceu um pedido de registro na agência chinesa, que deferiu, no último fim de semana. Estamos aguardando a tradução do parecer da agência chinesa para, com isso, complementar o nosso pedido no Brasil", informou Covas. A expectativa inicial, repassada pelo próprio diretor, era a de que o dossiê completo dos estudos da CoronaVac fosse enviado de forma simultânea na China e no Brasil.
Covas defendeu que o Butantan já envia documentos referentes à CoronaVac desde outubro, "a partir do processo de submissão contínua", junto à Agência Nacional de Vigilância Sanitária (Anvisa). "Assim que tivermos toda documentação, iniciaremos de fato a solicitação formal [do pedido de registro]", completou.
A partir da solicitação do pedido de registro definitivo, a Anvisa tem 60 dias para avaliar se registrará ou não o fármaco, permitindo a distribuição em massa das doses, bem como sua comercialização.
No entanto, por se tratar de uma vacina nova, assim como todas as outras iniciativas desenvolvidas para prevenir contra a covid-19, Covas frisou que, tecnicamente, todos os registros que podem ser concedidos neste momento são provisórios. "A vacina vira um produto, mas ainda tem que ser acompanhada até o final dos estudos clínicos, principalmente a chamada fase quatro, pós vacinação".
Registro definitivo
A Anvisa já recebeu um pedido de registro da vacina Covishield, conhecida popularmente como a vacina de Oxford/AstraZeneca. No Brasil, o imunizante é produzido pela Fundação Oswaldo Cruz (Fiocruz). Dois milhões de doses da Covishield, importadas da Índia, tiveram o uso emergencial aprovado pela agência brasileira.
A Pfizer também entrou com a solicitação do registro da vacina contra a covid-19 produzida pela empresa e não chegou a pedir pelo uso emergencial. Apesar da solicitação, a empresa não tem nenhum contrato firmado com o Ministério da Saúde para o fornecimento de doses do imunizante para o Brasil.
Saiba Mais
Notícias pelo celular
Receba direto no celular as notícias mais recentes publicadas pelo Correio Braziliense. É de graça. Clique aqui e participe da comunidade do Correio, uma das inovações lançadas pelo WhatsApp.
Dê a sua opinião
O Correio tem um espaço na edição impressa para publicar a opinião dos leitores. As mensagens devem ter, no máximo, 10 linhas e incluir nome, endereço e telefone para o e-mail sredat.df@dabr.com.br.
 Cidades DF
Cidades DF
 Cidades DF
Cidades DF