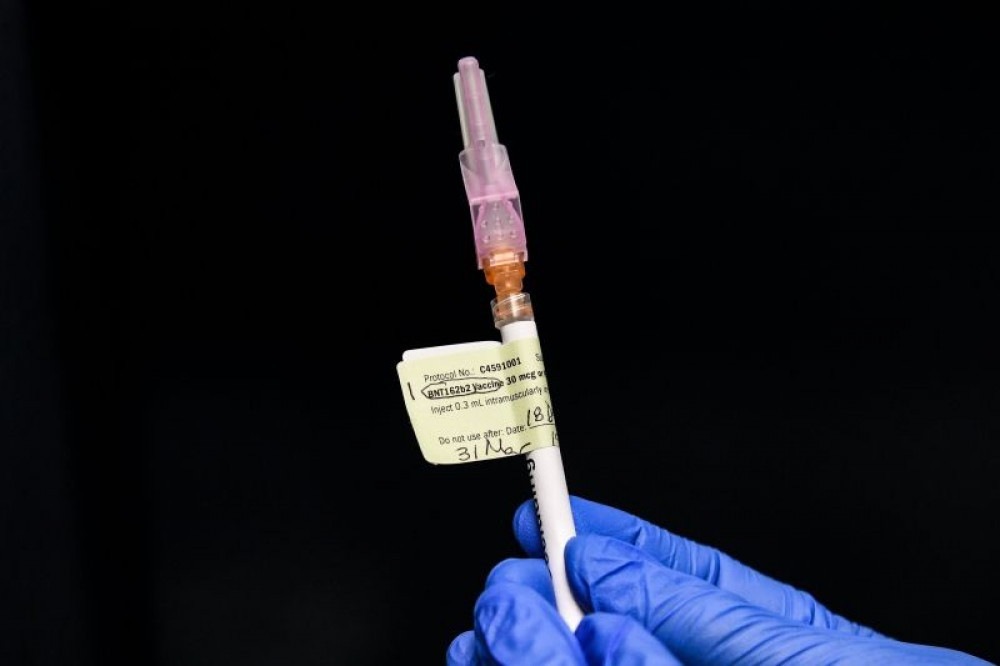
A Câmara dos Deputados aprovou, ontem, a Medida Provisória (MP) 1.003/20, que autoriza a adesão do Brasil ao Covax Facility, que permitirá ao país o acesso a 42,5 milhões de doses de vacinas contra a covid-19, suficientes para imunizar apenas 20% da população. Mas, apesar de a MP ser voltada para garantir a adesão ao consórcio internacional de imunizantes, com as alterações feitas pela Casa, o texto ficou mais amplo e flexibilizou as regras para que a Agência Nacional de Vigilância Sanitária (Anvisa) conceda autorização temporária de uso emergencial para importação, distribuição e uso de qualquer fármaco contra a covid-19.
Pelo texto, a autorização do organismo de controle deve ser concedida em até cinco dias, a partir do pedido feito pela desenvolvedora do imunizante, desde que pelo menos uma das nove entidades reguladoras internacionais incluídas na MP tenha aprovado o uso em seu território. As autoridades sanitárias internacionais listadas são as dos Estados Unidos (FDA), da União Europeia (EMA), do Japão (PMDA), da China (NMPA) –– que já constavam na lista para a autorização emergencial ––, do Canadá (HC), do Reino Unido (MHRA), da Coreia do Sul (KDCA), além do Ministério da Saúde da Rússia. A agência reguladora da Argentina (ANMAT) foi incluída no rol após a aprovação de destaque do proposto pelo PT.
Na última segunda-feira, a Anvisa estabeleceu que terá o prazo de até 10 dias para avaliar os pedidos que receberem para uso emergencial da vacina. Até o momento, nenhuma desenvolvedora de imunizantes solicitou pedido de uso emergencial.
Com as alterações feitas pela Câmara, a MP –– cujo texto segue para o Senado –– cria regras para a compra das vacinas e para o plano de imunização do Ministério da Saúde. O texto determina, ainda, que a imunização seja coordenada pelo Ministério da Saúde e siga alguns parâmetros elaborados pelo Conselho Nacional de Secretários de Saúde (Conass) e pelo Conselho Nacional de Secretarias Municipais de Saúde (Conasems).
Para as compras das vacinas, a MP libera R$ 2,5 bilhões, sendo R$ 711,7 milhões para as do Covax Facility, além de uma garantia financeira de R$ 91,8 milhões e pagamento adicional de R$ 1,71 milhão. Os recursos sairão do orçamento do Programa Nacional de Imunização (PNI).
A adesão brasileira ao consórcio não implica obrigatoriedade de compra das vacinas, que depende de uma análise técnica. Para o relator da MP, deputado Geninho Zuliani (DEM-SP), o Covax deve ser encarado como um caminho alternativo, já que o Brasil fechou acordos bilaterais com laboratórios. “Uma espécie de seguro, que pode ou não ser utilizado para ampliação de acesso e obtenção de número maior de doses”, descreveu.