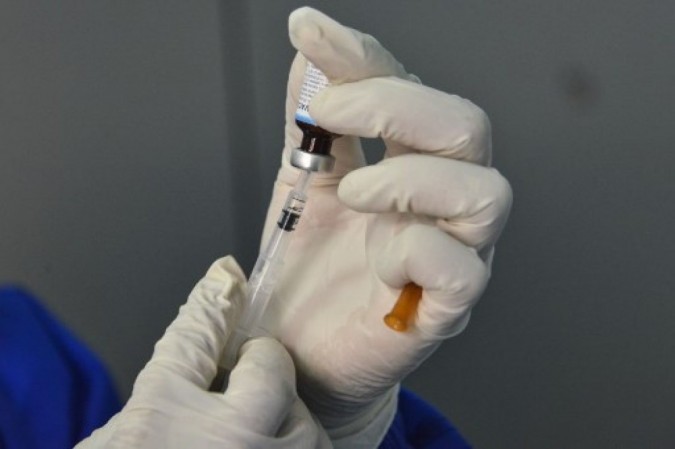
A Agência Nacional de Vigilância em Saúde (Anvisa) autorizou, nesta sexta-feira (18/9), a ampliação de mais um estudo de vacina contra a covid-19. Desta vez, a candidata norte-americana BNT162 com RNA anti-viral, da empresa Pfizer-Whyeth, passou pelo crivo da agência e terá o dobro de participantes para os testes, podendo contar com candidatos a partir de 16 anos.
Os testes estão sendo realizados na Bahia e em São Paulo e, com a atualização, contam com mil voluntários em cada um dos estados. Antes, somente pessoas acima de 18 anos estavam autorizados a participar. A solicitação de ampliação foi feita pelo laboratório Pfizer-Wyeth, responsável pelo desenvolvimento da vacina.
Outras candidatas
Segundo a Anvisa, "solicitações para a ampliação do número de voluntários, entre outras alterações, são comuns em testes clínicos". Esta é a segunda mudança autorizada pela agência em relação à candidata da Pfizer-Wyeth. Em 8 de setembro, a solicitação foi para autorização de mais um local de fabricação para a vacina testada.
Esta semana, a candidata de Oxford também recebeu aval para dobrar o número de testados e ampliar a faixa etária, incluindo idosos acima de 69 anos. A vacina produzida pela farmacêutica AstraZeneca dobrará o número de voluntários, passando de 5 mil para 10 mil participantes. Além disso, os testes passam a ser realizados, também, no Rio Grande do Norte e no Rio Grande do Sul, além de São Paulo, Rio de Janeiro e Bahia.
Notícias pelo celular
Receba direto no celular as notícias mais recentes publicadas pelo Correio Braziliense. É de graça. Clique aqui e participe da comunidade do Correio, uma das inovações lançadas pelo WhatsApp.
Dê a sua opinião
O Correio tem um espaço na edição impressa para publicar a opinião dos leitores. As mensagens devem ter, no máximo, 10 linhas e incluir nome, endereço e telefone para o e-mail sredat.df@dabr.com.br.
 Ciência e Saúde
Ciência e Saúde